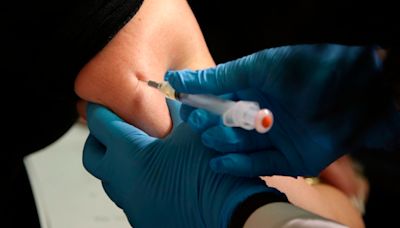
搜尋結果
- 擔心疫苗副作用。除了常見的急性不良反應,如手臂痠痛、發燒,還有血栓等嚴重不良反應外,有不少美國民眾擔心,疫苗恐對身體造成長期不良影響,尤其mRNA疫苗又是新技術。
- 疫苗產製時間太短。還有一些人,則是單純質疑疫苗產製的時間。過去的一般時期,不論是藥劑或疫苗,從研發到上市都得花上好幾年時間。但新冠肺炎疫苗的用途緊急,試驗階段恐不如以往嚴謹,施打也是採用緊急授權,而非FDA正式配發的藥證。
- 不認為病毒有威脅性。這是拒打理由中,最普遍的一個。即便封城超過一整年,依然有些民眾不把新冠肺炎當回事。他們或許明白感染風險的存在,但卻不認為病毒多有威脅性,尤其是年紀輕、身體較好的人,對自己的免疫力似乎都頗有信心。
- 施打環境仍不夠便利。如今在美國,打疫苗的門檻已經大大下降。近期剛從美返台的貿易業者黃先生分享:「在美國,幾乎每個藥局都可以接種疫苗,免費、而且大都不用預約。」
2022年3月10日 · 美國認可的疫苗廠牌包括輝瑞、莫德納、AZ、嬌生、諾瓦瓦克斯、科興、國藥、Covaxin,不包含高端。 台灣民眾入境美國前,須於搭機前1天內提供PCR採陰的英文版報告,抵達後3~5天也須接受抗原篩檢,並實施自我監測。
2022年9月5日 · 我們來看看國外的討論。 最近不到一個月內,歐洲、澳洲等先進國家先後核准已經不是主要流行病株的BA.1雙價次世代疫苗,「落後部署」引發一連串討論;台灣也在9月2 日核准莫德納的BA.1雙價次世代疫苗的緊急使用。 首先就會有人質疑:BA.1早已不是主要流行變異株了,為何不是核准現在正在肆虐的BA.5疫苗? 然而,了解目前美國已經核准的BA.5雙價疫苗其實只有根據動物試驗資料,就過關之後,民眾又擔心:這款沒有經過人體臨床試驗的疫苗安全嗎? 截至9月4日,美國是全球唯一核准BA.5雙價次世代疫苗的國家,核可時間在8月31日。 兩家研發BA.5疫苗的藥廠:莫德納與輝瑞BNT對於BA.5雙價疫苗目前都只做動物試驗,沒有人體臨床試驗數據。
2021年11月5日 · 美國疾病管制局(CDC)10月15日宣布,旅客未來入境美國,只要接種2劑疫苗(不限同一廠牌)後滿2週,登機前出示接種、採陰證明即可,且不必隔離,但仍須配合篩檢。
2021年7月16日 · 美國生技大廠諾瓦瓦克斯6月中旬宣布該公司研發的蛋白次單位新冠疫苗第3期臨床試驗數據,疫苗整體效力達90.4%,可100%預防中度或重症,對抗英國變種 (Alpha)、南非 (Beta)、巴西 (Gamma)及印度 (Delta)變異株效力達93%。 科學家兼醫藥作者巴斯廷(Hilda Bastian)在美國《大西洋(The Atlantic)》雜誌撰文指出,最先上市的mRNA疫苗非常棒,使用蛋白次單位技術的諾瓦瓦克斯又更好,她認為諾瓦瓦克斯是現在最好的新冠疫苗。 國產高端及聯亞疫苗也是蛋白次單位疫苗,可以據此類推,也具有高保護力及對抗變種病毒的能力嗎? (接種新冠疫苗已成全民運動,國產疫苗跟評價頗高的美國Novaxax疫苗同是蛋白次單位疫苗,是否值得期待也引發熱議。
2021年8月17日 · 美國生技大廠諾瓦瓦克斯(Novavax)8月初宣布,旗下新冠疫苗將延後上市,向食品藥物管理局(FDA)申請緊急使用授權(EUA)的時間,也會從秋季延後到年底。 消息一出,股價重挫、輿論譁然,讓這支「神級疫苗」光環瞬間黯淡。 3期試驗結果:副作用極輕微 保護力跟輝瑞一樣高. 諾瓦瓦克斯疫苗與高端、聯亞同屬「次單位蛋白疫苗」,運作原理是讓人體的免疫系統辨識棘蛋白,進而刺激免疫反應。 只不過,三者的抗原蛋白質來源不一樣。 高端、聯亞使用哺乳類倉鼠的細胞做培養,諾瓦瓦克斯則是使用秋行軍蟲的細胞。 推薦閱讀:與高端、聯亞同是蛋白疫苗諾瓦瓦克斯厲害之處在這裡. 次單位蛋白疫苗的共同優點,是 副作用少 。
2022年3月30日 · 美國食品藥物管理局FDA宣布,完成三劑接種的50歲以上成人,在間隔4個月之後就可接種第四劑疫苗,同時12歲以上免疫低下族群則可施打第五劑。 消息公布後,美國疾病管制預防中心CDC也同步更新疫苗接種指南,將第四劑接種列入正式的防疫建議。 美國FDA和CDC事先並未召開疫苗專家小組會議就逕自公布新措施,引發外界關注。 FDA的疫苗決策主要是根據下列的研究結果: 以色列最大的健保醫療服務機構Calit Health Services在Omicron流行期間,針對 50多萬名60歲以上的人口進行為期40天的研究,發現接種第四劑輝瑞疫苗者,比接種第三劑疫苗者的死亡率降低78%。